1.方法摘要
先以硝酸及硫酸分解镀液中的氰化物,使铜成为硫酸铜,在微酸性溶液中,铜离子和碘化钾定量地反应生成碘,用硫代硫酸钠滴定碘,可以测定铜含量,以淀粉 为指示剂。
2Cu2++4I-=2Cul↓+I₂
I₂+2Na2S203=Nal+Na2S406
淀粉和碘生成深蓝色碘一淀粉吸附物,终点到达后蓝色消失。淀粉指示剂应 在接近终点时加入,过早加入因碘一淀粉吸附物生成过多,则硫代硫酸钠和碘的反 应将变慢,不能得到正确的终点。碘化亚铜能吸附碘,使终点不明显,因此加入硫 氰酸铵,使碘化亚铜转化为溶解度更小的硫氰酸亚钢,不再吸附碘,可以敏锐地显 示终点。
Cu₂I2+2CNS-=2CuCNS↓+2I-
2.试剂
(1)硫酸相对密度1.84;
(2)硝酸相对密度1.42;
(3)氢氧化钠溶液100g/L;
(4)磷酸1+1;
(5)碘化钾溶液200g/L;
(6)硫氰酸铵溶液100g/L;
(7)氟化氢铵固体;
(8)淀粉指示剂 见试剂(128);
(9)0.1mol/L 硫代硫酸钠标准滴定溶液 见试剂(8)。
3.分析方法
吸取镀液1mL~2mL 于250mL锥形瓶中,加硫酸5mL及硝酸2mL,在通风橱内加热至冒浓白烟,此时溶液应呈蓝绿色,如带棕色,则有机物未分解完全,要再加 硫酸2mL~3mL 及硝酸1mL,再加热至冒白烟,冷却,小心加水50mL,摇动中滴加 氢氧化钠溶液至出现淡蓝色沉淀,加1+ 1 磷 酸 5mL,冷却,加入氟化氢铵3g,溶解摇匀,加碘化钾溶液15mL,立即以硫代硫酸钠标准滴定溶液滴定至浑浊的淡黄色,加淀粉指示剂5mL,继续滴定至蓝色将近消失,加硫氰酸铵溶液10mL,再滴定至乳白色为终点。
4. 计算
铜的质量浓度
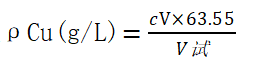
氰化亚铜的质量浓度
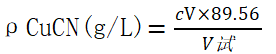
式中 c—— 硫代硫酸钠标准滴定溶液的浓度(mol/L);
V——消耗硫代硫酸钠标准滴定溶液的体积(mL);
V试——取样体积(mL);
63.55——Ar(Cu);
89.56——Mr(CuCN)。


Copyright © 2021 深圳市恒享表面处理技术有限公司 All Rights Reserved 备案号:粤ICP备09192382号 技术支持:易百讯 - 深圳网站建设